Polska była pierwszym krajem Europy Środkowo-Wschodniej, który wprowadził do praktyki klinicznej leczenie substytucyjne, przede wszystkim w związku z szybkim rozpowszechnieniem zakażeń HIV. Według danych PZH w 1991 roku osoby uzależnione od opiatów stanowiły 74,1% wszystkich osób zakażonych HIV. W 1992 roku w Instytucie Psychiatrii i Neurologii uruchomiono pierwszy, eksperymentalny program leczenia substytucyjnego.
30 lat leczenia substytucyjnego w Polsce
Wprowadzenie
Systematyczne badania nad możliwością wykorzystania metadonu w terapii osób uzależnionych od opioidów zostały zapoczątkowane przez Vincenta Dole’a i Marie Nyswander z Instytutu Rockefellera w Nowym Jorku już w latach 60. ubiegłego stulecia (Kreek, 1973). Stwierdzili oni, że po ustabilizowaniu dawki, metadon nie wywołuje efektu euforii i sedacji oraz nie upośledza funkcji poznawczych. W przypadku długotrwałego stosowania, metadon charakteryzuje się długim biologicznym okresem półtrwania, utrzymującym się powyżej 24 godzin. W terapii podtrzymującej poziom metadonu pozostaje względnie stały dzięki kontrolowanemu uwalnianiu do krwi z komórek wątroby. Mechanizm utrzymywania stałego poziomu leku we krwi powoduje, że receptory, z którymi wiąże się metadon, pozostają stale wysycone, a pacjent może normalnie funkcjonować (Dole, 1988). Metadon uwalnia także od poczucia „głodu” substancji i eliminuje objawy zespołu abstynencyjnego, co ma zasadnicze znaczenie w zapobieganiu nawrotom choroby i utrzymywaniu abstynencji od innych, niezleconych w terapii opioidów. Pacjenci z ustabilizowaną dawką leku mogą pozostawać na tej samej dawce przez wiele lat (Krantz & Mehler, 2004).
Początki leczenia substytucyjnego w Polsce
Polska była pierwszym krajem Europy Środkowo-Wschodniej, który wprowadził do praktyki klinicznej leczenie substytucyjne, przede wszystkim w związku z szybkim rozpowszechnieniem zakażeń HIV. Według danych PZH w 1991 roku osoby uzależnione od opiatów stanowiły 74,1% wszystkich osób zakażonych HIV (Szata, 1993). Najpopularniejszym opiatem był tzw. kompot (wyciąg ze słomy makowej, produkowany domowym sposobem), stosowany dożylnie. W 1992 roku w Instytucie Psychiatrii i Neurologii (IPiN) uruchomiono pierwszy, eksperymentalny program leczenia substytucyjnego. Lekarkami, które od początku były zaangażowane w uruchomienie tego programu była dr Celina Godwod-Sikorska i jej współpracownik Janusz Sierosławski, dr Karina Steinbarth-Chmielewska oraz dr Helena Furga-Baran. Program miał charakter projektu naukowo-badawczego, który zaplanowany był na pół roku: od czerwca 1992 do grudnia 1992 roku. W tym czasie program był finansowany przez Fundację Nauki Polskiej. Pod koniec 1992 roku zapadła decyzja o kontynuowaniu programu przez kolejny rok. Finansowanie na kontynuację zapewniło Ministerstwo Zdrowia i Opieki Społecznej (Godwod-Sikorska, 1994).
W zachodniej Europie pierwsze programy leczenia substytucyjnego powstały w latach 60. i 70. Do prekursorów należała m.in. Szwecja, Niderlandy, Wielka Brytania, Dania, Włochy. Znacznie później, bo w 1987 roku, terapia substytucyjna została zainicjowana w Niemczech i w Austrii. Lata 90. XX wieku to czas, w którym leczenie substytucyjne weszło do praktyki klinicznej w Chorwacji (1991 rok). W Grecji, Norwegii, Francji, Czechach i na Węgrzech leczenie substytucyjne wprowadzono później niż w Polsce, bo w drugiej połowie lat 90.
We wszystkich wymienionych krajach, wpływ na podjęcie decyzji o udostępnieniu terapii substytucyjnej miały niepokojące doniesienia o wysokim rozpowszechnieniu używania opioidów, znaczna liczba osób od nich uzależniona, ale przede wszystkim narastająca od lat 80. XX wieku epidemia HIV/AIDS.
Spory i dyskusje wokół leczenia substytucyjnego
Przygotowania do uruchomienia programu leczenia substytucyjnego w IPiN i pierwsze miesiące jego realizacji wiązały się z ogromnymi emocjami. Przede wszystkim projekt budził liczne kontrowersje w środowisku lekarzy psychiatrów, terapeutów uzależnień i wielu innych specjalistów zajmujących się osobami uzależnionymi. Przeciwnicy zarzucali leczeniu substytucyjnemu, że nie prowadzi do pełnej i trwałej abstynencji od opioidów i podtrzymuje uzależnienie. Oceniali leczenie substytucyjne jako etycznie wątpliwe. Zadawali pytanie, czy można kierować do terapii substytucyjnej „na rzecz utrzymania pacjenta w sytuacji mniejszego zła” (Karaczyńska & Sękiewicz, 1994). Szukając odpowiedzi na to pytanie, konstatowali, że nie można, bo kierując pacjenta do terapii substytucyjnej, dajemy mu co najwyżej szansę na „godne umieranie” (Karaczyńska & Sękiewicz, 1994). Z kolei zwolennicy leczenia substytucyjnego zwracali uwagę, że nieetyczne jest narażanie osób uzależnionych od opiatów na zakażenie wieloma chorobami i ryzyko przedwczesnego zgonu w sytuacji, gdy znane są metody terapii minimalizującej te ryzyka (Habrat i in., 1995), (WHO, 2004). Zwracano uwagę, że pacjenci uzależnieni od „kompotu” bardzo często przerywali leczenie w tradycyjnych ośrodkach terapii uzależnień i szybko wracali do destrukcyjnego, zagrażającego ich życiu nałogu.
Ta dychotomia w postrzeganiu i ocenie terapii substytucyjnej prowadziła do gorących sporów i dyskusji podczas konferencji czy na łamach prasy i czasopism naukowych, polaryzując środowisko. Po 30 latach prowadzenia leczenia substytucyjnego w Polsce intensywność tych sporów jest mniejsza, a niegdysiejsi przeciwnicy tej metody leczenia stali się często jej orędownikami. Dysponujemy obecnie bardzo wieloma wynikami badań naukowych, które jednoznacznie wskazują na korzyści i efekty leczenia substytucyjnego. Jednak nadal zbyt optymistycznym byłoby stwierdzenie, że leczenie substytucyjne uzyskało pełną akceptację wszystkich potencjalnych interesariuszy.
Leczenie substytucyjne z perspektywy personelu medycznego i pacjentów
W pamięci dr K. Steinbarth-Chmielewskiej i dr H. Furgi-Baran pierwsze tygodnie i miesiące programu leczenia substytucyjnego to przede wszystkim wielka satysfakcja, że po latach bezradnego przyglądania się wielokrotnym powrotom pacjentów uzależnionych od „kompotu” na oddział detoksykacyjny mogą obserwować, jak ich funkcjonowanie ulega systematycznej poprawie. Wielu z nich zrezygnowało z kradzieży i dealowania. Podejmowali bardziej systematyczną pracę, powracali do pełnienia ról społecznych, bardziej dbali o swoje zdrowie, prawie nie zakażali się HIV i innymi chorobami, jak HCV czy gruźlica. A przede wszystkim nie umierali z powodu przedawkowania. Personel medyczny opiekujący się pacjentami pierwszego programu substytucyjnego poczuł, że ta terapia przynosi efekty, których nigdy do tej pory nie udało się osiągnąć w tradycyjnych modelach terapii i po detoksykacji wobec tak dużej liczby pacjentów.
Z perspektywy pacjentów udział w programie był nobilitacją, wiedzieli, że na ich oczach dokonuje się wielka zmiana w dostępnych metodach terapii. Na pytanie, czy nie bali się poddać działaniu leku, który nie był stosowany do tej pory w Polsce, ci z którymi mogłam porozmawiać, odpowiadali, że nie. Słyszeli, że taka forma leczenia stosowana jest w innych krajach, np. w Holandii. Wiedzieli, że znosi głód narkotyku i umożliwia uwolnienie się od obsesyjnej myśli przyjęcia kolejnej dawki „kompotu”. U wielu z nich pojawił się promyk nadziei, że mogą mieć swoje życie pod większą kontrolą. Pacjenci, z którymi rozmawiałam, mówili też o wielkim lęku i niezadowoleniu, gdy po czterech miesiącach leczenia substytucyjnego lekarze zaczęli im stopniowo zmniejszać dawki metadonu, co było zgodne z pierwotnym założeniem, że program będzie trwał tylko pół roku. Zarówno lekarze, pacjenci i ich rodziny rozpoczęli walkę o przedłużenie programu. Zwrócono się do ówczesnego ministra zdrowia i opieki społecznej o przeznaczenie środków finansowych na kontynuowanie programu leczenia substytucyjnego. Lekarze odwoływali się do spektakularnych efektów, które uzyskano w czasie kilkumiesięcznej terapii metadonem i argumentowali, że leczenie, które jest skuteczne, zgodnie z podstawową zasadą w naukach medycznych, powinno być kontynuowane. Ostatecznie MZiOS podjęło decyzje o przeznaczeniu dodatkowych funduszy i tak program został przedłużony, a pacjenci, ich rodziny i personel odetchnęli z ulgą.
Założenia pierwszego programu leczenia metadonem
Do pierwszego programu leczenia substytucyjnego byli kwalifikowani pacjenci, którzy spełniali bardzo wygórowane kryteria:
- byli mieszkańcami Warszawy lub bliskich okolic,
- w wieku od 25 do 40 lat,
- uzależnieni od opiatów co najmniej 5 lat,
- wielokrotnie i bezskutecznie podejmujący leczenie (detoksykacja, rehabilitacja ukierunkowana na abstynencję) bez efektów,
- bez zaburzeń psychotycznych,
- bez zaburzeń psychoorganicznych,
- wyrazili zgodę na leczenie z zastosowaniem metadonu.
Do programu nie były przyjmowane kobiety w ciąży i osoby ze znacznymi zaburzeniami adaptacyjnymi oraz z tendencją do zachowań agresywnych (Godwod-Sikorska, 1994).
Od 1992 do 1997 roku leczenie substytucyjne prowadzone było na podstawie zezwolenia Ministerstwa Zdrowia i Opieki Społecznej. Jego losy nie były pewne aż do 1997 roku, kiedy to w Ustawie z dnia 24 kwietnia 1997 roku o przeciwdziałaniu narkomanii w art. 15 ust. 1 stwierdzano, że „osoba uzależniona może być leczona zgodnie z programem przewidującym stosowanie leczenia substytucyjnego”. 6 września 1999 roku po raz pierwszy minister zdrowia i opieki społecznej wydał rozporządzenie w sprawie leczenia substytucyjnego.
Co dziś wiemy o skuteczności leczenia substytucyjnego?
Ograniczenie zakażeń HIV
Podtrzymujące leczenie substytucyjne osób uzależnionych od opioidów odznacza się dużą skutecznością w zakresie minimalizowania ryzyka zakażenia HIV w przypadku osób niezakażonych. Osoby uczestniczące w terapii substytucyjnej co najmniej trzy miesiące i przyjmujące odpowiednio wysoką dawkę środka substytucyjnego zmniejszają liczbę iniekcji oraz rzadziej dzielą się sprzętem do iniekcji (Chmielewska i in., 1998), (WHO, 2003). Oszacowano, że udział w terapii substytucyjnej jest związany średnio z 54-procentową redukcją ryzyka zakażenia HIV wśród iniekcyjnych użytkowników opioidów (Mac-Arthur i in., 2012). Ponadto z badań wynika, że uczestnictwo w podtrzymującej terapii substytucyjnej iniekcyjnych użytkowników narkotyków już zakażonych HIV poprawia adherencję i wirologiczną odpowiedź na terapię antyretrowirusową, co może redukować ryzyko dalszej transmisji wirusa na populację użytkowników narkotyków i pozostałą część populacji (MacArthur i in., 2012). Wyniki niektórych badań sugerują, że połączenie podtrzymującego leczenia substytucyjnego z programem wymiany igieł i strzykawek może jeszcze w większym stopniu przyczynić się do ograniczenia ryzyka transmisji zakażenia HIV (Degenhardt i in., 2010).
Udział w podtrzymującej terapii substytucyjnej wpływa także na ograniczenie zachowań seksualnych wysokiego ryzyka, takich jak duża liczba partnerów seksualnych i sprzedawanie usług seksualnych za pieniądze, co z kolei przekłada się na ograniczenie ryzyka zakażenia HIV.
Ograniczenie zakażeń HCV i innych chorób zakaźnych
Terapia substytucyjna w istotny sposób przyczynia się do ograniczenia ryzyka zakażenia HCV, HBV oraz gruźlicy. Podobnie jak w przypadku ograniczenia zakażeń HIV, kluczowe znaczenie ma ograniczenie liczby przyjęć nielegalnych opioidów i zmniejszenie zachowań ryzykownych związanych z dzieleniem się sprzętem do iniekcji w trakcie leczenia substytucyjnego (Baran-Furga, 2001), (UNODC, 2015). Udział w terapii substytucyjnej ogranicza także ryzyko zakażenia żółtaczką typu B. W badaniach przeprowadzonych w programie leczenia substytucyjnego IPiN w Warszawie, wśród pacjentów uczestniczących rok w terapii substytucyjnej nie stwierdzono nowych przypadków zakażenia HBV (Baran-Furga, 2001).
Ograniczenie liczby zgonów
Podtrzymujące leczenie substytucyjne istotnie ogranicza umieralność wśród użytkowników opioidów (National Institutes of Health, 1997; Mathers i in., 2013). W badaniach przeprowadzonych w Wielkiej Brytanii na dużej próbie pacjentów objętych leczeniem substytucyjnym z użyciem metadonu i buprenorfiny w latach 1999−2005 (6252 pacjentów w wieku od 16 do 59 lat) wykazano, że współczynnik umieralności ogólnie był dwukrotnie wyższy wśród użytkowników opioidów pozostających poza leczeniem substytucyjnym w porównaniu z tymi, którzy uczestniczyli w terapii substytucyjnej (Cornish i in., 2010). Wpływ leczenia substytucyjnego na ograniczenie ryzyka zgonu wśród iniekcyjnych użytkowników opioidów udokumentowano także we Francji, gdzie po wprowadzeniu w 1995 roku buprenorfiny w podtrzymującej terapii substytucyjnej przepisywanej przez lekarzy pierwszego kontaktu, stwierdzono, że liczba zgonów z przedawkowania zmniejszyła się o 79% (Auriacombe i in., 2004).
Ogólna poprawa stanu zdrowia somatycznego i psychicznego
Pacjenci używający opioidów dożylnie zgłaszają się do programów leczenia substytucyjnego z wieloma problemami zdrowotnymi, wśród nich szczególnie częste są stany zapalne układu żylnego związane z częstymi iniekcjami dokonywanymi bez przestrzegania podstawowych zasad higieny. W badaniu przeprowadzonym w programie leczenia substytucyjnego IPiN stwierdzono występowanie u 19% pacjentów przy przyjęciu do programu zapalenie żył, owrzodzenia podudzi, ropnie na skórze. Po rocznej terapii substytucyjnej te zmiany chorobowe utrzymywały się tylko u 1% leczonych pacjentów. Nie stwierdzono także świeżego procesu zapalnego z tej przyczyny (Baran-Furga, 2001).
Poprawa funkcjonowania społecznego i jakości życia
Udział w terapii substytucyjnej ma pozytywny i znaczący wpływ na ograniczenie zachowań przestępczych przez użytkowników opioidów (Ward i in., 1999). Kwestię przestępczości osób uczestniczących w terapii substytucyjnej poddano badaniom m.in. w Polsce. Wyniki niepublikowanej pracy doktorskiej wskazują, że po rocznym okresie terapii substytucyjnej tylko niewielka liczba pacjentów leczonych w programie substytucyjnym kontynuowała działalność przestępczą – przed terapią było to 87% pacjentów, po roku terapii substytucyjnej – 7% pacjentów. Wraz ze zmniejszeniem się odsetka osób dokonujących przestępstw zwiększył się odsetek pacjentów korzystających z legalnych źródeł dochodu, takich jak praca dorywcza (odpowiednio z 11% do 27%) oraz renta lub zasiłek społeczny (odpowiednio z 43% do 74%; Baran-Furga, 2001).
Istotnym kryterium oceny programów leczenia substytucyjnego może być subiektywnie postrzegana przez pacjentów jakość ich życia. Kwestia ta została poddana ocenie w programie leczenia substytucyjnego w IPiN i Centrum Profilaktyki Uzależnień w Poznaniu. Po roku uczestniczenia w terapii substytucyjnej pacjenci raportowali znaczącą poprawę w takich wymiarach, jak funkcjonowanie społeczne, ograniczenia spowodowane stanem somatycznym, zdrowie psychiczne oraz energia i witalność (Habrat i in., 2002).
Cytowane wyniki znajdują odzwierciedlenie w wielu innych analizach, w tym w badaniu zatytułowanym National Treatment Outcome Research Study (NTORS), przeprowadzonym w Wielkiej Brytanii. Stwierdzono w nim, że po co najmniej rocznym udziale w terapii substytucyjnej nastąpiło zmniejszenie liczby popełnianych przestępstw przez osoby uczestniczące w niej o około 75 punktów procentowych. Uzyskane wskaźniki poprawy utrzymywały się w kolejnych pomiarach po 2, 4 i 5 latach uczestniczenia w terapii substytucyjnej. Podobne rezultaty uzyskano dla terapii stacjonarnej ukierunkowanej na utrzymanie abstynencji (Gossop, 2015), co wskazuje, że opłacalne jest inwestowanie w każdą z tych form leczenia. Każda z tych form terapii adresowana jest bowiem do innych grup pacjentów, charakteryzujących się różną motywacją do zmiany.
Polski model leczenia substytucyjnego i rozwiązania w innych krajach
Leczenie substytucyjne w Polsce od 30 lat opiera się na programach leczenia substytucyjnego prowadzonych w poradniach leczenia uzależnień. Warunkiem uruchomienia nowego programu jest uzyskanie pozytywnej opinii o programie od Dyrektora Krajowego Centrum Przeciwdziałania Uzależnieniom (wcześniej od Dyrektora Krajowego Biura ds. Przeciwdziałania Narkomanii) oraz uzyskanie zgody marszałka województwa właściwego ze względu na miejsce realizacji programu.
Wymagania, które musi spełnić pacjent kwalifikowany do podtrzymującego leczenia substytucyjnego, kilkakrotnie ulegały modyfikacjom w okresie 30 lat, adekwatnie do aktualnego stanu wiedzy i rekomendacji WHO. Obecnie pacjent powinien spełniać następujące wymagania:
- uzależnienie od opioidów,
- ukończenie 18. roku życia,
- wyrażenie zgody na podjęcie leczenia w ramach programu i przestrzeganie jego wymagań.
Kobiety w ciąży są przyjmowane w pierwszej kolejności do leczenia substytucyjnego, nie ma także wymogu dokumentowania wcześniejszych prób leczenia ukierunkowanych na abstynencję. Zaburzenia psychotyczne i psychoorganiczne nie stanowią już przeszkody do podjęcia terapii substytucyjnej.
Pacjentowi może być wydawany lek do domu, jeśli ten uczestniczy w terapii co najmniej sześć miesięcy. Przepisy przewidują także możliwość wcześniejszego wydawania pacjentowi leku do domu, jeśli przemawia za tym stan psychofizyczny pacjenta.
Na przestrzeni lat liczba pacjentów w programach substytucyjnych systematycznie rosła, choć nigdy nie osiągnęła wskaźników rekomendowanych przez Europejskie Centrum Monitorowania Narkotyków i Narkomanii.
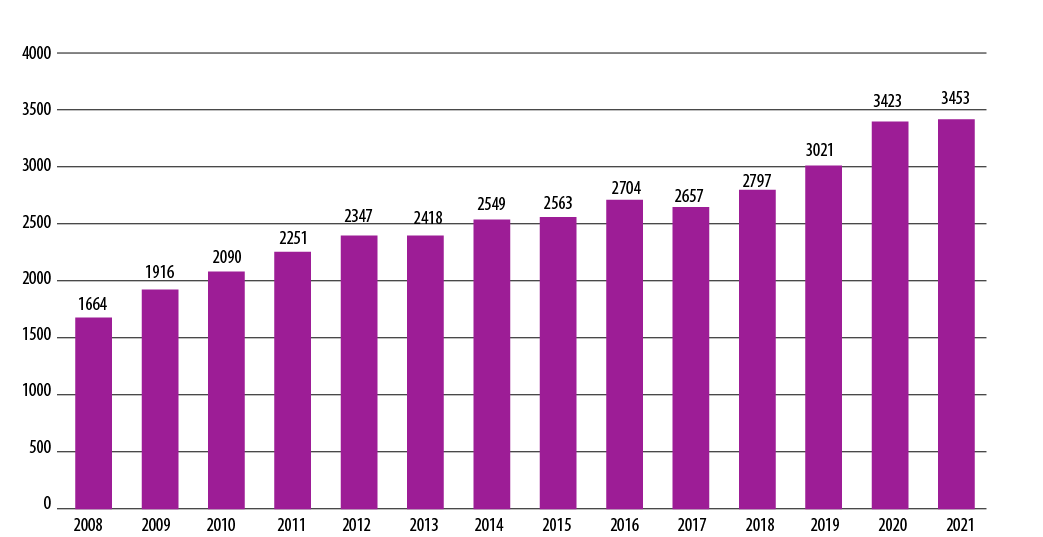
Biorąc pod uwagę ostatnie oszacowania liczby problemowych użytkowników opioidów w Polsce, można przyjąć, że liczba ta mieści się w szerokim przedziale 11 420–17 869. Środkowy punkt przedziału przypada na wartość 14 644 osób (Sierosławski, 2019), co oznacza że podtrzymującą terapią substytucyjną objętych było w 2021 roku między 19 a 30% osób uzależnionych od opioidów, najczęściej od heroiny.
Do chwili obecnej metadon jest najczęściej ordynowanym lekiem w terapii substytucyjnej. Przyjmuje go ok. 96% pacjentów leczonych substytucyjnie w naszym kraju. Buprenorfinę oraz morfinę o kontrolowanym uwalnianiu przyjmuje zaledwie około 4% leczonych osób (dane Krajowego Centrum Przeciwdziałania Uzależnieniom).
Pacjenci leczeni substytucyjnie nie ponoszą z tego tytułu żadnych opłat. Leczenie substytucyjne znajduje się bowiem w katalogu świadczeń gwarantowanych finansowanych przez NFZ. Pacjenci otrzymują bezpłatnie lek w podmiocie leczniczym. Leczenie substytucyjne jest bezpłatne zarówno dla pacjentów objętych składką ubezpieczenia zdrowotnego, jak i osób nieubezpieczonych. Kwestię osób nieubezpieczonych i ich prawo do bezpłatnych świadczeń zdrowotnych w zakresie leczenia uzależnienia regulują przepisy ustawy o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych.
Obecnie w Polsce funkcjonują 23 programy leczenia substytucyjnego, głównie zlokalizowane w dużych ośrodkach miejskich. W województwie podkarpackim i podlaskim przez 30 lat nie utworzono programów leczenia substytucyjnego.
Model leczenia substytucyjnego wdrażany w naszym kraju już wiele lat temu przestał być adekwatny do rzeczywistych potrzeb pacjentów. Ogranicza on dostęp do leczenia substytucyjnego oraz utrudnia proces reintegracji społecznej pacjentów (O Merrill, 2002).
W alternatywnych modelach leczenia substytucyjnego główny ciężar prowadzenia terapii przypada na lekarzy podstawowej opieki zdrowotnej, którzy w ramach ordynacji lekarskiej przepisują pacjentowi leki, w szczególności zawierające w swoim składzie buprenorfinę. W Austrii, Chorwacji, Francji i w Niemczech od 60 do 80% pacjentów leczonych jest substytucyjnie w ramach praktyk prowadzonych przez lekarzy ogólnych. Z wielu badań wynika, że takie rozwiązanie sprzyja dobrej dostępności leczenia substytucyjnego, w szczególności w mniejszych miejscowościach (Binder i in., 2016).
Rezultaty terapii prowadzonej w specjalistycznych poradniach leczenia uzależnień oraz przez lekarzy ogólnych są podobne (WHO, 2009).
Perspektywy rozwoju leczenia substytucyjnego w Polsce
W Polsce od lat trwa dyskusja nad wprowadzeniem zmian do organizacji leczenia substytucyjnego. Wskaźniki dostępności tej formy terapii w naszym kraju kształtują się na niskim poziomie. W większości krajów europejskich osiągnięto wysokie, bo co najmniej 50-procentowe, wskaźniki dostępności. We Francji wskaźnik ten jest najwyższy i kształtuje się na poziomie 70-80% osób problemowo używających opioidów objętych leczeniem substytucyjnym przy szacowanej liczbie problemowych użytkowników opioidów około 220 tys. osób. Niższą wartość wskaźnik ten osiągnął we Włoszech – około 60% i w Niemczech – około 50%, przy szacowanych populacjach problemowych użytkowników heroiny około 170 tys. w każdym z tych krajów. W Austrii, Grecji i Chorwacji szacuje się, że około 60% użytkowników opioidów objętych jest leczeniem substytucyjnym, natomiast populacje osób uzależnionych są nieporównanie mniejsze.
Już w 2017 roku ówczesne Krajowe Biuro ds. Przeciwdziałania Narkomanii przygotowało projekt ustawy o zmianie ustawy o przeciwdziałaniu narkomanii, który zakładał umożliwienie lekarzom podstawowej opieki zdrowotnej prowadzenie leczenia substytucyjnego produktami leczniczymi zawierającymi w swoim składzie buprenorfinę. Z tego projektu szybko się wycofano, głównie z powodu obaw, że liczba lekarzy podstawowej opieki zdrowotnej w polskim systemie opieki i leczenia jest niewystarczająca w stosunku do potrzeb systemu opieki zdrowotnej. Krytycy włączenia podstawowej opieki zdrowotnej w krąg podmiotów odpowiedzialnych za leczenie substytucyjne zwracali także uwagę na brak wystarczającego przygotowania lekarzy POZ do prowadzenia leczenia substytucyjnego. W związku z powyższym przygotowano nowy projekt ustawy o zmianie ustawy o przeciwdziałaniu narkomanii, który zakłada możliwość wystawiania recept na leki substytucyjne w ramach ordynacji lekarskiej zawierających substancję czynną buprenorfinę. Receptę na leki, zawierające w swoim składzie buprenorfinę, będzie mógł, zgodnie z projektem ustawy, wystawiać lekarz będący świadczeniodawcą albo lekarz zatrudniony lub wykonujący zawód u świadczeniodawcy, z którym Narodowy Fundusz Zdrowia zawarł umowę o udzielanie świadczeń opieki zdrowotnej w rodzaju opieka psychiatryczna i leczenie uzależnień. Stworzenie przepisów, które stwarzają realną szansę na wprowadzenie do leczenia substytucyjnego buprenorfiny, wpisuje się w rekomendacje Światowej Organizacji Zdrowia, która od wielu lat wyjaśnia, że stosowanie w terapii substytucyjnej więcej niż jednego leku umożliwia pacjentom, u których występują skutki uboczne stosowania jednego leku lub, którzy nie utrzymują się w terapii z zastosowaniem określonego leku, skorzystanie z leku alternatywnego. Zapewnienie możliwości wyboru leku może przyczyniać się do zwiększenia liczby osób pozostających w terapii substytucyjnej oraz podniesienia jej skuteczności poprzez lepsze dopasowanie leku do indywidualnych potrzeb pacjenta (WHO, 2001).
W przypadku wypisywania recepty do samodzielnej realizacji przez pacjenta nie bez znaczenia jest, że buprenorfina to lek o wyższym niż metadon profilu bezpieczeństwa (Bonhomme i in., 2012).
Projekt ustawy znosi także obowiązek uzyskiwania pozytywnej opinii Dyrektora Krajowego Centrum i zgody marszałka województwa na prowadzenie leczenia substytucyjnego w ramach ordynacji lekarskiej. Obowiązek ten nadal będzie spoczywał na poradniach leczenia uzależnień prowadzących programy leczenia substytucyjnego.
W celu wykluczenia udziału pacjenta w tym samym czasie w więcej niż jednym programie leczenia substytucyjnego oraz w leczeniu substytucyjnym w ramach ordynacji lekarskiej prowadzonej przez lekarza, projekt ustawy podtrzymuje obowiązek prowadzenia przez świadczeniodawcę Rejestru Pacjentów Objętych Leczeniem Substytucyjnym. Ponadto świadczeniodawca ma obowiązek zgłaszania pacjentów leczonych substytucyjnie do Ewidencji Zanonimizowanych Kodów Pacjentów Objętych Leczeniem Substytucyjnym prowadzonym przez Krajowe Centrum Przeciwdziałania Uzależnieniom.
Zarysowany powyżej projekt ustawy został zarekomendowany w październiku przez Komitet Stały Rady Ministrów. Projekt musi jeszcze zostać zaopiniowany przez Komisję Prawniczą, zaakceptowany przez Radę Ministrów, a następnie przyjęty przez parlament. Choć wydaje się, że to jeszcze długa droga, to mimo to nigdy dotąd zmiany organizacji leczenia substytucyjnego nie były tak bliskie realizacji.
Bibliografia
- Auriacombe, M. i in. (2004), „French Field Experience with Buprenorphine”, The American Journal on Addictions, 13(S1), pp. S17-S28.
- Baran-Furga, H. (2001), „Picie alkoholu przez pacjentów uzależnionych od opiatów leczonych substytucyjnie metadonem”, niepublikowana praca doktorska. IPiN, Warszawa.
- Bonhomme, J. i in. (2012), „Opioid Addiction and Abuse in Primary Care Practice: A comparison of methadone and Buprenorphine as Treatment Options”, Journal of Natl Medical Association, 104(0), pp. 342-350.
- Chmielewska, K., Baran, H., Dąbrowski, S. & Habrat, B. (1999), „Kontynuowanie terapii w programie substytucyjnego leczenia metadonem przez pacjentów uzależnionych od opiatów”, Alkoholizm i Narkomania, 32(3).
- Cornish, R. i in. (2010), „Risk of death during and after opiate substitution treatment in primary care: prospective observational study in UK General Practice Research Databas”, BMJ, 26 10., Volume 341.
- Degenhardt, L. i in. (2010), „Prevention of HIV infection for people who inject drugs: Why individual, structural, and combination of approaches are needed”, Lancet, pp. 285-301.
- Dole, V.P. (1988), „Implications of Methadone Maintenance for Theories of Narcotic Addiction”, JAMA, Volume 260, pp. 3025-3029.
- Godwod-Sikorska, C. (1994), „Ocena wdrażania terapii metadonem w zapobieganiu HIV/AIDS wśród narkomanów opiatowych”, Alkoholizm i Narkomania, 1(15), pp. 19-24.
- Gossop, M. (2015), „The National Treatment Outcomes Research Study (NTORS) and its influence on addiction treatment policy in the United Kingdom”, Addiction. Supplement Article, Volume 110, pp. 50-53.
- Habrat, B., Steinbarth-Chmielewska, K. & Baran-Furga, H. (1995), „Programy metadonowe-niektóre mity i fakty”, Problemy Alkoholizmu, Issue 1, pp. 9-10.
- Karaczyńska, B. & Sękiewicz, J. (1994), „Przeciw metadonowi. In: Program metadonowy na tle innych programów rehabilitacyjnych osób uzależnionych w profilaktyce HIV/AIDS”, Warszawa: Biuro ds. Narkomanii.
- Kreek, M.J. (1973), „Medical Safety and Side Effects of Methadone in Tolerant Individuals”, The Journal of the American Medical Association, 223(6), pp. 665-668.
- Krantz, M.J. & Mehler, P. S. (2004), „Treating Opioid Dependence. Growing Implications for Primary Care”, Arch Intern Med, 164(3), pp. 277-288.
- Mathers, B.M. i in. (2013), „Mortality among people who inject drugs: a systematic review and meta-analysis”, Bull World Health Organ., 1 February, 91(2), pp. 102-123.
- MacArthur, G.J. i in. (2012), „Opiate substitution treatment and HIV transmission in people who inject drugs: systematic review and meta-analysis”, BMJ.
- Sierosławski, J. (2019), „Oszacowanie liczby problemowych użytkowników narkotyków”, Dokument nieopublikowany.
- Szata, W. (1993), „Zakażenia HIV i zachorowania AIDS w Polsce w latach 1985-1992”, Alkoholizm i Narkomania, Volume Wydanie specjalne: Zagrożenia AIDS, pp. 89-101.
- Szukalski, B. (1997), „Opiaty naturalne i syntetyczne”, Alkoholizm i Narkomania, 29(4), pp. 529-548.
- UNODC, 2015. World Drug Report, Viena: UNITED NATIONS OFFICE ON DRUGS AND CRIME (UNODC).
- WHO, 2004. Neuroscience of psychoactive substance use and dependence. s.l.:World Health Organization, Geneva.
- WHO, 2001. Zapewnienie równowagi polityk krajowych dotyczących substancji kontrolowanych, Genewa: Światowa Organizacja Zdrowia.
